Alfafold 3: revolucionar la estructura molecular y la predicción de la interacción
Desde su lanzamiento en 2020, más de 2 millones de investigadores han recurrido a AlphaFold 2 de Google DeepMind para predecir estructuras de proteínas, ayudando en avances como el desarrollo de vacunas y tratamientos contra el cáncer. Este modelo abordó un desafío que desconcertó a los científicos durante más de medio siglo. Pero el equipo de Google DeepMind no se detuvo ahí; en lugar de descansar en sus laureles, se arremangaron y comenzaron a trabajar en AlphaFold 3.
Lanzado en mayo por Google DeepMind e Isomorphic Labs, AlphaFold 3 eleva el nivel. No solo predice el plegamiento de proteínas; también pronostica la estructura y las interacciones de todo tipo de moléculas de la vida, incluyendo ADN, ARN y ligandos, esas pequeñas moléculas que se unen a las proteínas.
"Con AlphaFold 2, hicimos grandes avances en resolver el rompecabezas del plegamiento de proteínas, pero la comunidad científica ha pasado a cosas más complejas," explica Jonas Adler, científico investigador en Google DeepMind. "Los investigadores ahora exploran detalles como cómo se unen las moléculas pequeñas o cómo funciona el ARN, áreas donde AlphaFold 2 se quedó corto. Para seguir el ritmo de lo último en biología y química, necesitábamos una herramienta que pudiera manejar todo tipo de biomoléculas."
"Todo" aquí incluye ligandos, que son cruciales porque constituyen aproximadamente la mitad de todos los fármacos. "En Isomorphic Labs, vemos el enorme potencial de AlphaFold 3 para diseñar fármacos de manera racional, y ya lo estamos utilizando todos los días," dice Adrian Stecula, líder de investigación en Isomorphic Labs. "Estamos explorando cómo las nuevas moléculas pequeñas se unen a nuevos objetivos farmacológicos, descubriendo cómo las proteínas interactúan con ADN y ARN, y estudiando cómo los ajustes químicos afectan las estructuras de las proteínas; el nuevo modelo abre todas estas posibilidades."
Incorporar estos tipos de moléculas adicionales significó lidiar con muchas más combinaciones. "Las proteínas son bastante sencillas; solo hay 20 aminoácidos estándar," señala Jonas. "Pero las moléculas pequeñas? Son muy variadas, con infinitas posibilidades. Son súper diversas."
Dándose cuenta de que una base de datos completa era imposible, el equipo lanzó AlphaFold Server. Esta herramienta gratuita permite a los científicos ingresar sus propias secuencias, y AlphaFold genera los complejos moleculares para ellos. Desde que se lanzó en mayo, se ha utilizado para crear más de 1 millón de estructuras.
"Es como Google Maps pero para complejos moleculares," dice Lindsay Willmore, ingeniera de investigación en Google DeepMind. "Incluso si no eres programador, puedes simplemente copiar y pegar tus secuencias de proteínas, ADN, ARN o moléculas pequeñas, presionar un botón y esperar unos minutos. Obtendrás tu estructura junto con métricas de confianza para ayudarte a evaluar la predicción."
Para hacer que AlphaFold 3 funcione con una gama tan amplia de biomoléculas, el equipo amplió los datos de entrenamiento para incluir ADN, ARN, moléculas pequeñas y más. "Pensamos, '¿Por qué no entrenar con todo en nuestro conjunto de datos que nos ayudó con las proteínas y ver hasta dónde podemos llegar?'" explica Lindsay. "Resulta que llegamos bastante lejos."
Un cambio clave en AlphaFold 3 fue en la parte final del modelo que crea la estructura. Mientras que AlphaFold 2 usaba un módulo complejo basado en geometría, AlphaFold 3 cambió a un modelo generativo más simple basado en difusión, similar a otros modelos avanzados de generación de imágenes como Imagen. Este cambio simplificó cómo el modelo maneja los nuevos tipos de moléculas.
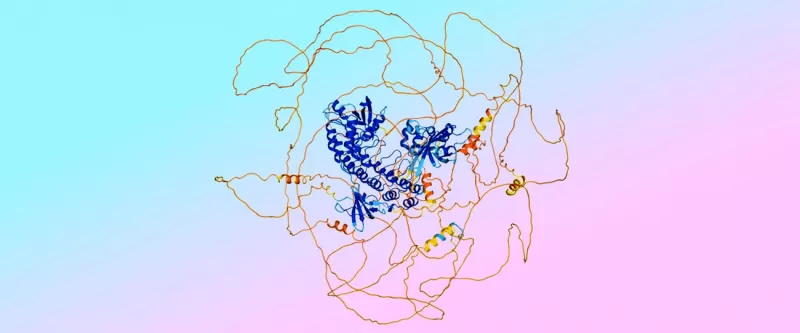
Sin embargo, este cambio trajo un nuevo desafío: el modelo de difusión creaba erróneamente una estructura "ordenada" para regiones de proteínas que en realidad son "desordenadas"—piensa en intentar organizar un montón de espagueti caótico en una espiral ordenada.
Entonces, el equipo recurrió a AlphaFold 2, que destaca en predecir estas interacciones desordenadas. "Usamos esas predicciones de AlphaFold 2 para entrenar a AlphaFold 3, enseñándole a reconocer y predecir el desorden," dice Lindsay.
"Tenemos un dicho: 'Confía en el fusilli, rechaza el espagueti,'" añade Jonas con una risita.
Un ejemplo de una predicción de AlphaFold 3, mostrando regiones ordenadas de "fusilli" en azul y regiones desordenadas de "espagueti" en naranja. Los colores indican la confianza del modelo en la precisión de la predicción.
El equipo está emocionado de ver cómo se usará AlphaFold 3 en campos como la genómica y el diseño de fármacos. "Es increíble ver hasta dónde hemos llegado," dice Jonas. "Lo que antes era difícil ahora es fácil, y lo que era imposible ahora está al alcance. Todavía hay problemas difíciles de resolver, pero estamos emocionados por lo que AlphaFold 3 puede ayudarnos a lograr."
 "Dot AI Companion App anuncia su cierre y suspende el servicio personalizado"
Dot, una aplicación de inteligencia artificial diseñada para funcionar como amigo personal y confidente, dejará de funcionar, según anunciaron el viernes sus desarrolladores. New Computer, la empresa
"Dot AI Companion App anuncia su cierre y suspende el servicio personalizado"
Dot, una aplicación de inteligencia artificial diseñada para funcionar como amigo personal y confidente, dejará de funcionar, según anunciaron el viernes sus desarrolladores. New Computer, la empresa
 Anthropic resuelve un caso de piratería de libros generados por inteligencia artificial
Anthropic ha llegado a una resolución en un importante litigio sobre derechos de autor con autores estadounidenses, aceptando una propuesta de acuerdo de demanda colectiva que evita un juicio potencia
Anthropic resuelve un caso de piratería de libros generados por inteligencia artificial
Anthropic ha llegado a una resolución en un importante litigio sobre derechos de autor con autores estadounidenses, aceptando una propuesta de acuerdo de demanda colectiva que evita un juicio potencia
 Figma pone a disposición de todos los usuarios su herramienta de creación de aplicaciones basada en inteligencia artificial
Figma Make, la innovadora plataforma de desarrollo "prompt-to-app" presentada a principios de este año, ha salido oficialmente de la fase beta y se ha puesto a disposición de todos los usuarios. Esta
comentario (21)
0/200
Figma pone a disposición de todos los usuarios su herramienta de creación de aplicaciones basada en inteligencia artificial
Figma Make, la innovadora plataforma de desarrollo "prompt-to-app" presentada a principios de este año, ha salido oficialmente de la fase beta y se ha puesto a disposición de todos los usuarios. Esta
comentario (21)
0/200
![HarryClark]() HarryClark
HarryClark
 21 de agosto de 2025 09:01:19 GMT+02:00
21 de agosto de 2025 09:01:19 GMT+02:00
AlphaFold 3 sounds like a game-changer! Predicting molecular interactions could speed up drug discovery big time. Curious how it stacks up against traditional lab methods. 🧬


 0
0
![PeterThomas]() PeterThomas
PeterThomas
 17 de agosto de 2025 01:01:00 GMT+02:00
17 de agosto de 2025 01:01:00 GMT+02:00
AlphaFold 3 sounds like a game-changer! Predicting molecular interactions with such precision could really speed up drug discovery. I'm curious how it stacks up against traditional lab methods in terms of cost and time. Anyone know? 🤔


 0
0
![JoseLewis]() JoseLewis
JoseLewis
 14 de agosto de 2025 13:00:59 GMT+02:00
14 de agosto de 2025 13:00:59 GMT+02:00
AlphaFold 3 sounds like a game-changer! Predicting molecular interactions could speed up drug discovery big time. Excited to see how it shapes medical breakthroughs! 🚀


 0
0
![ElijahCollins]() ElijahCollins
ElijahCollins
 14 de agosto de 2025 05:01:00 GMT+02:00
14 de agosto de 2025 05:01:00 GMT+02:00
AlphaFold 3 sounds like a game-changer! Predicting molecular interactions could speed up drug discovery big time. Curious how it stacks against human researchers—will it outsmart us or just make our coffee breaks longer? 😄


 0
0
![GregorySmith]() GregorySmith
GregorySmith
 6 de agosto de 2025 04:01:00 GMT+02:00
6 de agosto de 2025 04:01:00 GMT+02:00
AlphaFold 3 sounds like a game-changer! Predicting molecular interactions with such precision could unlock new frontiers in medicine. But I wonder, will this tech stay accessible to all researchers, or get locked behind paywalls? 🤔


 0
0
![BruceThomas]() BruceThomas
BruceThomas
 1 de agosto de 2025 08:08:50 GMT+02:00
1 de agosto de 2025 08:08:50 GMT+02:00
AlphaFold 3 sounds like a game-changer for science! Predicting molecular interactions could speed up drug discovery big time. Excited to see where this goes! 🚀


 0
0

Desde su lanzamiento en 2020, más de 2 millones de investigadores han recurrido a AlphaFold 2 de Google DeepMind para predecir estructuras de proteínas, ayudando en avances como el desarrollo de vacunas y tratamientos contra el cáncer. Este modelo abordó un desafío que desconcertó a los científicos durante más de medio siglo. Pero el equipo de Google DeepMind no se detuvo ahí; en lugar de descansar en sus laureles, se arremangaron y comenzaron a trabajar en AlphaFold 3.
Lanzado en mayo por Google DeepMind e Isomorphic Labs, AlphaFold 3 eleva el nivel. No solo predice el plegamiento de proteínas; también pronostica la estructura y las interacciones de todo tipo de moléculas de la vida, incluyendo ADN, ARN y ligandos, esas pequeñas moléculas que se unen a las proteínas.
"Con AlphaFold 2, hicimos grandes avances en resolver el rompecabezas del plegamiento de proteínas, pero la comunidad científica ha pasado a cosas más complejas," explica Jonas Adler, científico investigador en Google DeepMind. "Los investigadores ahora exploran detalles como cómo se unen las moléculas pequeñas o cómo funciona el ARN, áreas donde AlphaFold 2 se quedó corto. Para seguir el ritmo de lo último en biología y química, necesitábamos una herramienta que pudiera manejar todo tipo de biomoléculas."
"Todo" aquí incluye ligandos, que son cruciales porque constituyen aproximadamente la mitad de todos los fármacos. "En Isomorphic Labs, vemos el enorme potencial de AlphaFold 3 para diseñar fármacos de manera racional, y ya lo estamos utilizando todos los días," dice Adrian Stecula, líder de investigación en Isomorphic Labs. "Estamos explorando cómo las nuevas moléculas pequeñas se unen a nuevos objetivos farmacológicos, descubriendo cómo las proteínas interactúan con ADN y ARN, y estudiando cómo los ajustes químicos afectan las estructuras de las proteínas; el nuevo modelo abre todas estas posibilidades."
Incorporar estos tipos de moléculas adicionales significó lidiar con muchas más combinaciones. "Las proteínas son bastante sencillas; solo hay 20 aminoácidos estándar," señala Jonas. "Pero las moléculas pequeñas? Son muy variadas, con infinitas posibilidades. Son súper diversas."
"Es como Google Maps pero para complejos moleculares," dice Lindsay Willmore, ingeniera de investigación en Google DeepMind. "Incluso si no eres programador, puedes simplemente copiar y pegar tus secuencias de proteínas, ADN, ARN o moléculas pequeñas, presionar un botón y esperar unos minutos. Obtendrás tu estructura junto con métricas de confianza para ayudarte a evaluar la predicción."
Para hacer que AlphaFold 3 funcione con una gama tan amplia de biomoléculas, el equipo amplió los datos de entrenamiento para incluir ADN, ARN, moléculas pequeñas y más. "Pensamos, '¿Por qué no entrenar con todo en nuestro conjunto de datos que nos ayudó con las proteínas y ver hasta dónde podemos llegar?'" explica Lindsay. "Resulta que llegamos bastante lejos."
Un cambio clave en AlphaFold 3 fue en la parte final del modelo que crea la estructura. Mientras que AlphaFold 2 usaba un módulo complejo basado en geometría, AlphaFold 3 cambió a un modelo generativo más simple basado en difusión, similar a otros modelos avanzados de generación de imágenes como Imagen. Este cambio simplificó cómo el modelo maneja los nuevos tipos de moléculas.
Sin embargo, este cambio trajo un nuevo desafío: el modelo de difusión creaba erróneamente una estructura "ordenada" para regiones de proteínas que en realidad son "desordenadas"—piensa en intentar organizar un montón de espagueti caótico en una espiral ordenada.
Entonces, el equipo recurrió a AlphaFold 2, que destaca en predecir estas interacciones desordenadas. "Usamos esas predicciones de AlphaFold 2 para entrenar a AlphaFold 3, enseñándole a reconocer y predecir el desorden," dice Lindsay.
"Tenemos un dicho: 'Confía en el fusilli, rechaza el espagueti,'" añade Jonas con una risita.
El equipo está emocionado de ver cómo se usará AlphaFold 3 en campos como la genómica y el diseño de fármacos. "Es increíble ver hasta dónde hemos llegado," dice Jonas. "Lo que antes era difícil ahora es fácil, y lo que era imposible ahora está al alcance. Todavía hay problemas difíciles de resolver, pero estamos emocionados por lo que AlphaFold 3 puede ayudarnos a lograr."
 Anthropic resuelve un caso de piratería de libros generados por inteligencia artificial
Anthropic ha llegado a una resolución en un importante litigio sobre derechos de autor con autores estadounidenses, aceptando una propuesta de acuerdo de demanda colectiva que evita un juicio potencia
Anthropic resuelve un caso de piratería de libros generados por inteligencia artificial
Anthropic ha llegado a una resolución en un importante litigio sobre derechos de autor con autores estadounidenses, aceptando una propuesta de acuerdo de demanda colectiva que evita un juicio potencia
 Figma pone a disposición de todos los usuarios su herramienta de creación de aplicaciones basada en inteligencia artificial
Figma Make, la innovadora plataforma de desarrollo "prompt-to-app" presentada a principios de este año, ha salido oficialmente de la fase beta y se ha puesto a disposición de todos los usuarios. Esta
Figma pone a disposición de todos los usuarios su herramienta de creación de aplicaciones basada en inteligencia artificial
Figma Make, la innovadora plataforma de desarrollo "prompt-to-app" presentada a principios de este año, ha salido oficialmente de la fase beta y se ha puesto a disposición de todos los usuarios. Esta
 21 de agosto de 2025 09:01:19 GMT+02:00
21 de agosto de 2025 09:01:19 GMT+02:00
AlphaFold 3 sounds like a game-changer! Predicting molecular interactions could speed up drug discovery big time. Curious how it stacks up against traditional lab methods. 🧬


 0
0
 17 de agosto de 2025 01:01:00 GMT+02:00
17 de agosto de 2025 01:01:00 GMT+02:00
AlphaFold 3 sounds like a game-changer! Predicting molecular interactions with such precision could really speed up drug discovery. I'm curious how it stacks up against traditional lab methods in terms of cost and time. Anyone know? 🤔


 0
0
 14 de agosto de 2025 13:00:59 GMT+02:00
14 de agosto de 2025 13:00:59 GMT+02:00
AlphaFold 3 sounds like a game-changer! Predicting molecular interactions could speed up drug discovery big time. Excited to see how it shapes medical breakthroughs! 🚀


 0
0
 14 de agosto de 2025 05:01:00 GMT+02:00
14 de agosto de 2025 05:01:00 GMT+02:00
AlphaFold 3 sounds like a game-changer! Predicting molecular interactions could speed up drug discovery big time. Curious how it stacks against human researchers—will it outsmart us or just make our coffee breaks longer? 😄


 0
0
 6 de agosto de 2025 04:01:00 GMT+02:00
6 de agosto de 2025 04:01:00 GMT+02:00
AlphaFold 3 sounds like a game-changer! Predicting molecular interactions with such precision could unlock new frontiers in medicine. But I wonder, will this tech stay accessible to all researchers, or get locked behind paywalls? 🤔


 0
0
 1 de agosto de 2025 08:08:50 GMT+02:00
1 de agosto de 2025 08:08:50 GMT+02:00
AlphaFold 3 sounds like a game-changer for science! Predicting molecular interactions could speed up drug discovery big time. Excited to see where this goes! 🚀


 0
0