«Алфалолд 3: Революция молекулярной структуры и прогнозирования взаимодействия»
С момента запуска в 2020 году более 2 миллионов исследователей использовали AlphaFold 2 от Google DeepMind для предсказания структур белков, что способствовало прорывам в разработке вакцин и лечении рака. Эта модель решила проблему, которая озадачивала учёных более полувека. Но команда Google DeepMind не остановилась на достигнутом; вместо того чтобы почивать на лаврах, они закатали рукава и начали работать над AlphaFold 3.
Запущенная в мае Google DeepMind и Isomorphic Labs, AlphaFold 3 поднимает планку. Она не только предсказывает свёртывание белков, но и прогнозирует структуру и взаимодействия всех видов молекул жизни, включая ДНК, РНК и лиганды — те крошечные молекулы, которые связываются с белками.
«С AlphaFold 2 мы сделали огромные шаги в решении загадки свёртывания белков, но научное сообщество перешло к более сложным задачам», — объясняет Йонас Адлер, научный сотрудник Google DeepMind. «Исследователи теперь углубляются в детали, такие как связывание малых молекул или работа РНК, где AlphaFold 2 была недостаточно эффективна. Чтобы идти в ногу с последними достижениями в биологии и химии, нам нужен был инструмент, способный работать со всеми видами биомолекул».
«Всё» здесь включает лиганды, которые важны, поскольку составляют около половины всех лекарств. «В Isomorphic Labs мы видим огромный потенциал AlphaFold 3 для рационального дизайна лекарств, и мы уже используем её ежедневно», — говорит Адриан Стецула, руководитель исследований в Isomorphic Labs. «Мы изучаем, как новые малые молекулы связываются с новыми мишенями для лекарств, как белки взаимодействуют с ДНК и РНК, и как химические изменения влияют на структуры белков — новая модель открывает все эти возможности».
Включение этих дополнительных типов молекул означало работу с огромным количеством комбинаций. «Белки довольно просты; есть только 20 стандартных аминокислот», — отмечает Йонас. «Но малые молекулы? Они повсюду, с бесконечными возможностями. Они чрезвычайно разнообразны».
Понимая, что создание полной базы данных невозможно, команда запустила AlphaFold Server. Этот бесплатный инструмент позволяет учёным вводить свои последовательности, и AlphaFold генерирует молекулярные комплексы для них. С момента запуска в мае он был использован для создания более 1 миллиона структур.
«Это как Google Maps, но для молекулярных комплексов», — говорит Линдси Уиллмор, инженер-исследователь в Google DeepMind. «Даже если вы не программист, вы можете просто скопировать и вставить последовательности белков, ДНК, РНК или малых молекул, нажать кнопку и подождать несколько минут. Вы получите структуру вместе с метриками уверенности, чтобы оценить точность предсказания».
Чтобы AlphaFold 3 работала с таким широким спектром биомолекул, команда расширила обучающие данные, включив ДНК, РНК, малые молекулы и многое другое. «Мы подумали: „Почему бы не обучить модель на всём, что помогло нам с белками, и посмотреть, как далеко мы сможем зайти?“» — объясняет Линдси. «Оказалось, мы зашли довольно далеко».
Ключевое изменение в AlphaFold 3 произошло в финальной части модели, создающей структуру. Если AlphaFold 2 использовала сложный модуль на основе геометрии, то AlphaFold 3 перешла на более простую генеративную модель, основанную на диффузии, подобную другим продвинутым моделям генерации изображений, таким как Imagen. Это изменение упростило обработку новых типов молекул.
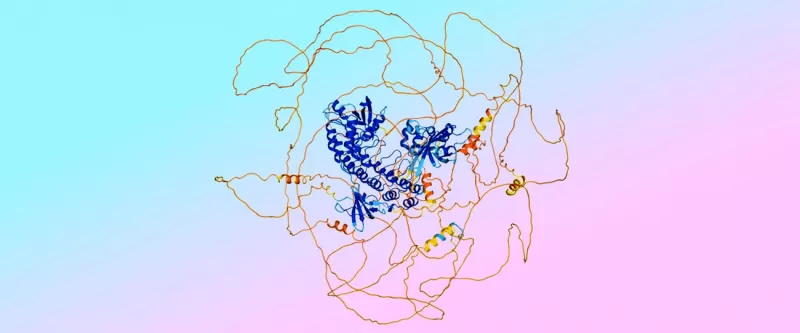
Однако этот переход принёс новую проблему: диффузионная модель ошибочно создавала «упорядоченную» структуру для регионов белков, которые на самом деле «неупорядочены» — представьте, что вы пытаетесь организовать кучу хаотичных спагетти в аккуратную спираль.
Поэтому команда обратилась к AlphaFold 2, которая отлично предсказывает эти неупорядоченные взаимодействия. «Мы использовали предсказания AlphaFold 2 для обучения AlphaFold 3, научив её распознавать и предсказывать неупорядоченность», — говорит Линдси.
«У нас есть поговорка: „Доверяй фузилли, отвергай спагетти“», — добавляет Йонас с улыбкой.
Пример предсказания от AlphaFold 3, показывающий упорядоченные регионы «фузилли» в синем цвете и неупорядоченные регионы «спагетти» в оранжевом. Цвета указывают на уверенность модели в точности предсказания.
Команда с энтузиазмом смотрит на то, как AlphaFold 3 будет использоваться в таких областях, как геномика и разработка лекарств. «Удивительно видеть, как далеко мы продвинулись», — говорит Йонас. «То, что раньше было сложным, теперь легко, а то, что было невозможным, теперь в пределах досягаемости. Всё ещё есть трудные задачи, но мы в восторге от того, чего может достичь AlphaFold 3».
 WordPress.com теперь позволяет ИИ-ботам создавать и публиковать посты, а также выполнять другие задачи
WordPress.com, популярная платформа для веб-хостинга и публикации контента, теперь внедряет ИИ-агентов — шаг, который может кардинально изменить облик и функциональность Интернета. В пятницу компания
WordPress.com теперь позволяет ИИ-ботам создавать и публиковать посты, а также выполнять другие задачи
WordPress.com, популярная платформа для веб-хостинга и публикации контента, теперь внедряет ИИ-агентов — шаг, который может кардинально изменить облик и функциональность Интернета. В пятницу компания
 Kakao Mobility представляет план развития автономного вождения 4-го уровня с использованием физического ИИ
Компания Kakao Mobility планирует самостоятельно разрабатывать технологии автономного вождения 4-го уровня в рамках своей стратегии «физического ИИ».На конференции World IT Show 2026, прошедшей в сеу
Kakao Mobility представляет план развития автономного вождения 4-го уровня с использованием физического ИИ
Компания Kakao Mobility планирует самостоятельно разрабатывать технологии автономного вождения 4-го уровня в рамках своей стратегии «физического ИИ».На конференции World IT Show 2026, прошедшей в сеу
 Барри Диллер: доверие к Сэму Альтману теряет значение по мере приближения эры общей искусственной интеллигенции
Миллиардер и медиа-магнат Барри Диллер не считает генерального директора OpenAI Сэма Альтмана недостойным доверия, несмотря на недавние сообщения, свидетельствующие об обратном. Выступая на этой недел
Рекомендации по связанным специальным темам
Комментарии (21)
Барри Диллер: доверие к Сэму Альтману теряет значение по мере приближения эры общей искусственной интеллигенции
Миллиардер и медиа-магнат Барри Диллер не считает генерального директора OpenAI Сэма Альтмана недостойным доверия, несмотря на недавние сообщения, свидетельствующие об обратном. Выступая на этой недел
Рекомендации по связанным специальным темам
Комментарии (21)
![HarryClark]()
AlphaFold 3 sounds like a game-changer! Predicting molecular interactions could speed up drug discovery big time. Curious how it stacks up against traditional lab methods. 🧬
![PeterThomas]()
AlphaFold 3 sounds like a game-changer! Predicting molecular interactions with such precision could really speed up drug discovery. I'm curious how it stacks up against traditional lab methods in terms of cost and time. Anyone know? 🤔
![JoseLewis]()
AlphaFold 3 sounds like a game-changer! Predicting molecular interactions could speed up drug discovery big time. Excited to see how it shapes medical breakthroughs! 🚀
![ElijahCollins]()
AlphaFold 3 sounds like a game-changer! Predicting molecular interactions could speed up drug discovery big time. Curious how it stacks against human researchers—will it outsmart us or just make our coffee breaks longer? 😄
![GregorySmith]()
AlphaFold 3 sounds like a game-changer! Predicting molecular interactions with such precision could unlock new frontiers in medicine. But I wonder, will this tech stay accessible to all researchers, or get locked behind paywalls? 🤔

С момента запуска в 2020 году более 2 миллионов исследователей использовали AlphaFold 2 от Google DeepMind для предсказания структур белков, что способствовало прорывам в разработке вакцин и лечении рака. Эта модель решила проблему, которая озадачивала учёных более полувека. Но команда Google DeepMind не остановилась на достигнутом; вместо того чтобы почивать на лаврах, они закатали рукава и начали работать над AlphaFold 3.
Запущенная в мае Google DeepMind и Isomorphic Labs, AlphaFold 3 поднимает планку. Она не только предсказывает свёртывание белков, но и прогнозирует структуру и взаимодействия всех видов молекул жизни, включая ДНК, РНК и лиганды — те крошечные молекулы, которые связываются с белками.
«С AlphaFold 2 мы сделали огромные шаги в решении загадки свёртывания белков, но научное сообщество перешло к более сложным задачам», — объясняет Йонас Адлер, научный сотрудник Google DeepMind. «Исследователи теперь углубляются в детали, такие как связывание малых молекул или работа РНК, где AlphaFold 2 была недостаточно эффективна. Чтобы идти в ногу с последними достижениями в биологии и химии, нам нужен был инструмент, способный работать со всеми видами биомолекул».
«Всё» здесь включает лиганды, которые важны, поскольку составляют около половины всех лекарств. «В Isomorphic Labs мы видим огромный потенциал AlphaFold 3 для рационального дизайна лекарств, и мы уже используем её ежедневно», — говорит Адриан Стецула, руководитель исследований в Isomorphic Labs. «Мы изучаем, как новые малые молекулы связываются с новыми мишенями для лекарств, как белки взаимодействуют с ДНК и РНК, и как химические изменения влияют на структуры белков — новая модель открывает все эти возможности».
Включение этих дополнительных типов молекул означало работу с огромным количеством комбинаций. «Белки довольно просты; есть только 20 стандартных аминокислот», — отмечает Йонас. «Но малые молекулы? Они повсюду, с бесконечными возможностями. Они чрезвычайно разнообразны».
«Это как Google Maps, но для молекулярных комплексов», — говорит Линдси Уиллмор, инженер-исследователь в Google DeepMind. «Даже если вы не программист, вы можете просто скопировать и вставить последовательности белков, ДНК, РНК или малых молекул, нажать кнопку и подождать несколько минут. Вы получите структуру вместе с метриками уверенности, чтобы оценить точность предсказания».
Чтобы AlphaFold 3 работала с таким широким спектром биомолекул, команда расширила обучающие данные, включив ДНК, РНК, малые молекулы и многое другое. «Мы подумали: „Почему бы не обучить модель на всём, что помогло нам с белками, и посмотреть, как далеко мы сможем зайти?“» — объясняет Линдси. «Оказалось, мы зашли довольно далеко».
Ключевое изменение в AlphaFold 3 произошло в финальной части модели, создающей структуру. Если AlphaFold 2 использовала сложный модуль на основе геометрии, то AlphaFold 3 перешла на более простую генеративную модель, основанную на диффузии, подобную другим продвинутым моделям генерации изображений, таким как Imagen. Это изменение упростило обработку новых типов молекул.
Однако этот переход принёс новую проблему: диффузионная модель ошибочно создавала «упорядоченную» структуру для регионов белков, которые на самом деле «неупорядочены» — представьте, что вы пытаетесь организовать кучу хаотичных спагетти в аккуратную спираль.
Поэтому команда обратилась к AlphaFold 2, которая отлично предсказывает эти неупорядоченные взаимодействия. «Мы использовали предсказания AlphaFold 2 для обучения AlphaFold 3, научив её распознавать и предсказывать неупорядоченность», — говорит Линдси.
«У нас есть поговорка: „Доверяй фузилли, отвергай спагетти“», — добавляет Йонас с улыбкой.
Команда с энтузиазмом смотрит на то, как AlphaFold 3 будет использоваться в таких областях, как геномика и разработка лекарств. «Удивительно видеть, как далеко мы продвинулись», — говорит Йонас. «То, что раньше было сложным, теперь легко, а то, что было невозможным, теперь в пределах досягаемости. Всё ещё есть трудные задачи, но мы в восторге от того, чего может достичь AlphaFold 3».
 WordPress.com теперь позволяет ИИ-ботам создавать и публиковать посты, а также выполнять другие задачи
WordPress.com, популярная платформа для веб-хостинга и публикации контента, теперь внедряет ИИ-агентов — шаг, который может кардинально изменить облик и функциональность Интернета. В пятницу компания
WordPress.com теперь позволяет ИИ-ботам создавать и публиковать посты, а также выполнять другие задачи
WordPress.com, популярная платформа для веб-хостинга и публикации контента, теперь внедряет ИИ-агентов — шаг, который может кардинально изменить облик и функциональность Интернета. В пятницу компания
 Барри Диллер: доверие к Сэму Альтману теряет значение по мере приближения эры общей искусственной интеллигенции
Миллиардер и медиа-магнат Барри Диллер не считает генерального директора OpenAI Сэма Альтмана недостойным доверия, несмотря на недавние сообщения, свидетельствующие об обратном. Выступая на этой недел
Барри Диллер: доверие к Сэму Альтману теряет значение по мере приближения эры общей искусственной интеллигенции
Миллиардер и медиа-магнат Барри Диллер не считает генерального директора OpenAI Сэма Альтмана недостойным доверия, несмотря на недавние сообщения, свидетельствующие об обратном. Выступая на этой недел
AlphaFold 3 sounds like a game-changer! Predicting molecular interactions could speed up drug discovery big time. Curious how it stacks up against traditional lab methods. 🧬
AlphaFold 3 sounds like a game-changer! Predicting molecular interactions with such precision could really speed up drug discovery. I'm curious how it stacks up against traditional lab methods in terms of cost and time. Anyone know? 🤔
AlphaFold 3 sounds like a game-changer! Predicting molecular interactions could speed up drug discovery big time. Excited to see how it shapes medical breakthroughs! 🚀
AlphaFold 3 sounds like a game-changer! Predicting molecular interactions could speed up drug discovery big time. Curious how it stacks against human researchers—will it outsmart us or just make our coffee breaks longer? 😄
AlphaFold 3 sounds like a game-changer! Predicting molecular interactions with such precision could unlock new frontiers in medicine. But I wonder, will this tech stay accessible to all researchers, or get locked behind paywalls? 🤔


















 Дом
Дом























