Alphafold 3 : 분자 구조 및 상호 작용 예측 혁명
2020년 출시 이후, 200만 명 이상의 연구자들이 Google DeepMind의 AlphaFold 2를 사용하여 단백질 구조를 예측하며 백신 개발과 암 치료 같은 돌파구를 마련했습니다. 이 모델은 반세기 이상 과학자들을 당황하게 했던 문제를 해결했습니다. 하지만 Google DeepMind 팀은 여기서 멈추지 않고 소매를 걷어붙이고 AlphaFold 3 작업을 시작했습니다.
Google DeepMind와 Isomorphic Labs가 5월에 출시한 AlphaFold 3는 한 단계 더 나아갑니다. 단백질 접힘을 예측할 뿐만 아니라 DNA, RNA, 리간드 등 생명의 모든 분자의 구조와 상호작용을 예측합니다.
"AlphaFold 2로 단백질 접힘 퍼즐을 크게 풀었지만, 과학계는 더 복잡한 문제로 넘어갔습니다,"라고 Google DeepMind의 연구 과학자 Jonas Adler가 설명합니다. "연구자들은 이제 소분자가 어떻게 결합하는지, RNA가 어떻게 작동하는지와 같은 세부 사항을 탐구하고 있습니다. AlphaFold 2가 부족했던 영역입니다. 생물학과 화학의 최신 동향을 따라가기 위해 모든 종류의 생체 분자를 처리할 수 있는 도구가 필요했습니다."
여기서 "모든 것"은 약물의 약 절반을 차지하는 리간드를 포함합니다. "Isomorphic Labs에서 우리는 AlphaFold 3의 합리적인 약물 설계 가능성을 보고 있으며, 이미 매일 사용하고 있습니다,"라고 Isomorphic Labs의 연구 리더 Adrian Stecula가 말합니다. "우리는 새로운 소분자가 새로운 약물 표적에 어떻게 결합하는지, 단백질이 DNA와 RNA와 어떻게 상호작용하는지, 화학적 조정이 단백질 구조에 어떤 영향을 미치는지를 탐구하고 있습니다. 새 모델은 이 모든 가능성을 열어줍니다."
이러한 추가 분자 유형을 포함한다는 것은 훨씬 더 많은 조합을 처리해야 함을 의미했습니다. "단백질은 비교적 단순합니다. 표준 아미노산은 20개뿐입니다,"라고 Jonas가 말합니다. "하지만 소분자는? 무한한 가능성이 있습니다. 매우 다양합니다."
종합적인 데이터베이스가 불가능하다는 것을 깨닫고, 팀은 AlphaFold Server를 출시했습니다. 이 무료 도구는 과학자들이 자신의 서열을 입력하면 AlphaFold가 분자 복합체를 생성합니다. 5월 출시 이후 100만 개 이상의 구조를 생성했습니다.
"분자 복합체를 위한 Google Maps 같은 것입니다,"라고 Google DeepMind의 연구 엔지니어 Lindsay Willmore가 말합니다. "코더가 아니더라도 단백질, DNA, RNA 또는 소분자 서열을 복사해서 붙여넣고 버튼을 누르면 몇 분 기다리면 됩니다. 예측의 정확성을 평가하는 데 도움이 되는 신뢰도 지표와 함께 구조를 얻을 수 있습니다."
AlphaFold 3가 다양한 생체 분자와 작동하도록, 팀은 DNA, RNA, 소분자 등을 포함하도록 훈련 데이터를 확장했습니다. "단백질에 도움이 되었던 데이터셋의 모든 것을 훈련에 사용해보자는 생각을 했습니다,"라고 Lindsay가 설명합니다. "결과적으로 꽤 멀리 갔습니다."
AlphaFold 3의 주요 변화는 구조를 생성하는 모델의 마지막 부분에 있었습니다. AlphaFold 2는 복잡한 사용자 지정 기하학 기반 모듈을 사용했지만, AlphaFold 3는 Imagen과 같은 고급 이미지 생성 모델과 유사한 더 간단한 확산 기반 생성 모델로 전환했습니다. 이 변화는 모델이 새로운 분자 유형을 처리하는 방식을 간소화했습니다.
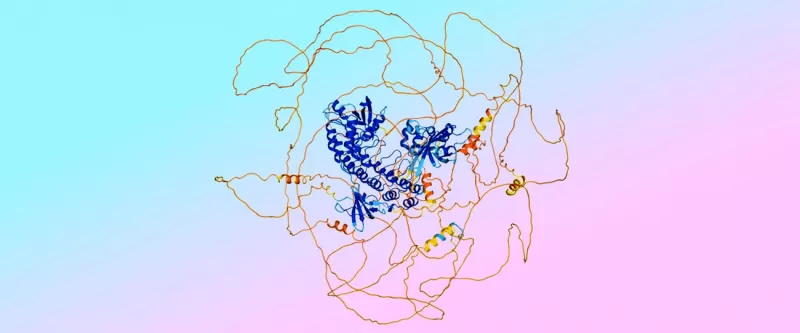
하지만 이 전환은 새로운 도전을 가져왔습니다. 확산 모델은 실제로 "무질서한" 단백질 영역을 잘못된 "질서 있는" 구조로 만들어냈습니다. 혼란스러운 스파게티 더미를 깔끔한 나선으로 정리하려는 것과 같습니다.
그래서 팀은 이러한 무질서한 상호작용 예측에 탁월한 AlphaFold 2로 눈을 돌렸습니다. "우리는 AlphaFold 2의 예측을 사용해 AlphaFold 3를 훈련시켜 무질서를 인식하고 예측하도록 가르쳤습니다,"라고 Lindsay가 말합니다.
"우리는 '푸실리를 믿고, 스파게티를 거부하라'는 말을 합니다,"라고 Jonas가 웃으며 덧붙입니다.
AlphaFold 3의 예측 예시로, 질서 있는 "푸실리" 영역은 파란색, 무질서한 "스파게티" 영역은 주황색으로 표시됩니다. 색상은 예측 정확도에 대한 모델의 신뢰도를 나타냅니다.
팀은 AlphaFold 3가 유전체학 및 약물 설계 분야에서 어떻게 사용될지 기대하고 있습니다. "우리가 얼마나 멀리 왔는지 놀랍습니다,"라고 Jonas가 말합니다. "한때 어려웠던 것은 이제 쉽고, 불가능했던 것은 이제 가능합니다. 여전히 풀어야 할 어려운 과제가 있지만, AlphaFold 3가 우리를 어디로 데려갈지 기쁩니다."
 카카오 모빌리티, 물리적 AI를 위한 레벨 4 자율주행 로드맵 제시
카카오모빌리티는 물리적 AI 전략의 일환으로 레벨 4 자율주행 기술을 자체 개발할 계획이다.서울 코엑스에서 열린 '2026 월드 IT 쇼' 컨퍼런스에서 카카오모빌리티의 김진규 부사장 겸 피지컬 AI 사업본부장은 로드맵을 발표했다. 그의 발표는 피지컬 AI 시대의 모빌리티 플랫폼을 기반으로 한 자율주행 서비스에 중점을 두었다.연합뉴스에 따르면, '아이디어
카카오 모빌리티, 물리적 AI를 위한 레벨 4 자율주행 로드맵 제시
카카오모빌리티는 물리적 AI 전략의 일환으로 레벨 4 자율주행 기술을 자체 개발할 계획이다.서울 코엑스에서 열린 '2026 월드 IT 쇼' 컨퍼런스에서 카카오모빌리티의 김진규 부사장 겸 피지컬 AI 사업본부장은 로드맵을 발표했다. 그의 발표는 피지컬 AI 시대의 모빌리티 플랫폼을 기반으로 한 자율주행 서비스에 중점을 두었다.연합뉴스에 따르면, '아이디어
 배리 딜러: AGI 시대가 다가옴에 따라 샘 알트먼에 대한 신뢰는 무의미하다
억만장자 미디어 거물 배리 딜러는 최근 보도에서 달리 제기된 주장에도 불구하고, 오픈AI의 샘 알트만 CEO가 신뢰할 수 없는 인물이라고 생각하지 않는다고 밝혔다. 이번 주 월스트리트저널(WSJ)이 주최한 ‘Future of Everything’ 컨퍼런스에서 연설한 딜러는, 일부 전직 동료들과 이사회 구성원들로부터 때때로 교묘하게 조종하거나 기만적이라는 비
배리 딜러: AGI 시대가 다가옴에 따라 샘 알트먼에 대한 신뢰는 무의미하다
억만장자 미디어 거물 배리 딜러는 최근 보도에서 달리 제기된 주장에도 불구하고, 오픈AI의 샘 알트만 CEO가 신뢰할 수 없는 인물이라고 생각하지 않는다고 밝혔다. 이번 주 월스트리트저널(WSJ)이 주최한 ‘Future of Everything’ 컨퍼런스에서 연설한 딜러는, 일부 전직 동료들과 이사회 구성원들로부터 때때로 교묘하게 조종하거나 기만적이라는 비
 유튜브, 정치인·공직자·언론인을 대상으로 AI 딥페이크 탐지 기능 확대
화요일, 유튜브는 딥페이크 탐지 기술을 일부 정부 관계자, 정치 후보자 및 언론인 대상으로 확대한다고 발표했다. 이 도구는 AI로 생성된 유사 영상을 식별하며, 시범 운영 참여자들은 유튜브 정책을 위반한다고 판단되는 무단 콘텐츠의 삭제를 요청할 수 있다.이 탐지 시스템은 초기 테스트 단계를 거친 후, 작년 유튜브 파트너 프로그램에 가입된 약 400만 명의
관련 특별 주제 추천
의견 (21)
0/500
유튜브, 정치인·공직자·언론인을 대상으로 AI 딥페이크 탐지 기능 확대
화요일, 유튜브는 딥페이크 탐지 기술을 일부 정부 관계자, 정치 후보자 및 언론인 대상으로 확대한다고 발표했다. 이 도구는 AI로 생성된 유사 영상을 식별하며, 시범 운영 참여자들은 유튜브 정책을 위반한다고 판단되는 무단 콘텐츠의 삭제를 요청할 수 있다.이 탐지 시스템은 초기 테스트 단계를 거친 후, 작년 유튜브 파트너 프로그램에 가입된 약 400만 명의
관련 특별 주제 추천
의견 (21)
0/500
![HarryClark]()
AlphaFold 3 sounds like a game-changer! Predicting molecular interactions could speed up drug discovery big time. Curious how it stacks up against traditional lab methods. 🧬
![PeterThomas]()
AlphaFold 3 sounds like a game-changer! Predicting molecular interactions with such precision could really speed up drug discovery. I'm curious how it stacks up against traditional lab methods in terms of cost and time. Anyone know? 🤔
![JoseLewis]()
AlphaFold 3 sounds like a game-changer! Predicting molecular interactions could speed up drug discovery big time. Excited to see how it shapes medical breakthroughs! 🚀
![ElijahCollins]()
AlphaFold 3 sounds like a game-changer! Predicting molecular interactions could speed up drug discovery big time. Curious how it stacks against human researchers—will it outsmart us or just make our coffee breaks longer? 😄
![GregorySmith]()
AlphaFold 3 sounds like a game-changer! Predicting molecular interactions with such precision could unlock new frontiers in medicine. But I wonder, will this tech stay accessible to all researchers, or get locked behind paywalls? 🤔

2020년 출시 이후, 200만 명 이상의 연구자들이 Google DeepMind의 AlphaFold 2를 사용하여 단백질 구조를 예측하며 백신 개발과 암 치료 같은 돌파구를 마련했습니다. 이 모델은 반세기 이상 과학자들을 당황하게 했던 문제를 해결했습니다. 하지만 Google DeepMind 팀은 여기서 멈추지 않고 소매를 걷어붙이고 AlphaFold 3 작업을 시작했습니다.
Google DeepMind와 Isomorphic Labs가 5월에 출시한 AlphaFold 3는 한 단계 더 나아갑니다. 단백질 접힘을 예측할 뿐만 아니라 DNA, RNA, 리간드 등 생명의 모든 분자의 구조와 상호작용을 예측합니다.
"AlphaFold 2로 단백질 접힘 퍼즐을 크게 풀었지만, 과학계는 더 복잡한 문제로 넘어갔습니다,"라고 Google DeepMind의 연구 과학자 Jonas Adler가 설명합니다. "연구자들은 이제 소분자가 어떻게 결합하는지, RNA가 어떻게 작동하는지와 같은 세부 사항을 탐구하고 있습니다. AlphaFold 2가 부족했던 영역입니다. 생물학과 화학의 최신 동향을 따라가기 위해 모든 종류의 생체 분자를 처리할 수 있는 도구가 필요했습니다."
여기서 "모든 것"은 약물의 약 절반을 차지하는 리간드를 포함합니다. "Isomorphic Labs에서 우리는 AlphaFold 3의 합리적인 약물 설계 가능성을 보고 있으며, 이미 매일 사용하고 있습니다,"라고 Isomorphic Labs의 연구 리더 Adrian Stecula가 말합니다. "우리는 새로운 소분자가 새로운 약물 표적에 어떻게 결합하는지, 단백질이 DNA와 RNA와 어떻게 상호작용하는지, 화학적 조정이 단백질 구조에 어떤 영향을 미치는지를 탐구하고 있습니다. 새 모델은 이 모든 가능성을 열어줍니다."
이러한 추가 분자 유형을 포함한다는 것은 훨씬 더 많은 조합을 처리해야 함을 의미했습니다. "단백질은 비교적 단순합니다. 표준 아미노산은 20개뿐입니다,"라고 Jonas가 말합니다. "하지만 소분자는? 무한한 가능성이 있습니다. 매우 다양합니다."
"분자 복합체를 위한 Google Maps 같은 것입니다,"라고 Google DeepMind의 연구 엔지니어 Lindsay Willmore가 말합니다. "코더가 아니더라도 단백질, DNA, RNA 또는 소분자 서열을 복사해서 붙여넣고 버튼을 누르면 몇 분 기다리면 됩니다. 예측의 정확성을 평가하는 데 도움이 되는 신뢰도 지표와 함께 구조를 얻을 수 있습니다."
AlphaFold 3가 다양한 생체 분자와 작동하도록, 팀은 DNA, RNA, 소분자 등을 포함하도록 훈련 데이터를 확장했습니다. "단백질에 도움이 되었던 데이터셋의 모든 것을 훈련에 사용해보자는 생각을 했습니다,"라고 Lindsay가 설명합니다. "결과적으로 꽤 멀리 갔습니다."
AlphaFold 3의 주요 변화는 구조를 생성하는 모델의 마지막 부분에 있었습니다. AlphaFold 2는 복잡한 사용자 지정 기하학 기반 모듈을 사용했지만, AlphaFold 3는 Imagen과 같은 고급 이미지 생성 모델과 유사한 더 간단한 확산 기반 생성 모델로 전환했습니다. 이 변화는 모델이 새로운 분자 유형을 처리하는 방식을 간소화했습니다.
하지만 이 전환은 새로운 도전을 가져왔습니다. 확산 모델은 실제로 "무질서한" 단백질 영역을 잘못된 "질서 있는" 구조로 만들어냈습니다. 혼란스러운 스파게티 더미를 깔끔한 나선으로 정리하려는 것과 같습니다.
그래서 팀은 이러한 무질서한 상호작용 예측에 탁월한 AlphaFold 2로 눈을 돌렸습니다. "우리는 AlphaFold 2의 예측을 사용해 AlphaFold 3를 훈련시켜 무질서를 인식하고 예측하도록 가르쳤습니다,"라고 Lindsay가 말합니다.
"우리는 '푸실리를 믿고, 스파게티를 거부하라'는 말을 합니다,"라고 Jonas가 웃으며 덧붙입니다.
팀은 AlphaFold 3가 유전체학 및 약물 설계 분야에서 어떻게 사용될지 기대하고 있습니다. "우리가 얼마나 멀리 왔는지 놀랍습니다,"라고 Jonas가 말합니다. "한때 어려웠던 것은 이제 쉽고, 불가능했던 것은 이제 가능합니다. 여전히 풀어야 할 어려운 과제가 있지만, AlphaFold 3가 우리를 어디로 데려갈지 기쁩니다."
 배리 딜러: AGI 시대가 다가옴에 따라 샘 알트먼에 대한 신뢰는 무의미하다
억만장자 미디어 거물 배리 딜러는 최근 보도에서 달리 제기된 주장에도 불구하고, 오픈AI의 샘 알트만 CEO가 신뢰할 수 없는 인물이라고 생각하지 않는다고 밝혔다. 이번 주 월스트리트저널(WSJ)이 주최한 ‘Future of Everything’ 컨퍼런스에서 연설한 딜러는, 일부 전직 동료들과 이사회 구성원들로부터 때때로 교묘하게 조종하거나 기만적이라는 비
배리 딜러: AGI 시대가 다가옴에 따라 샘 알트먼에 대한 신뢰는 무의미하다
억만장자 미디어 거물 배리 딜러는 최근 보도에서 달리 제기된 주장에도 불구하고, 오픈AI의 샘 알트만 CEO가 신뢰할 수 없는 인물이라고 생각하지 않는다고 밝혔다. 이번 주 월스트리트저널(WSJ)이 주최한 ‘Future of Everything’ 컨퍼런스에서 연설한 딜러는, 일부 전직 동료들과 이사회 구성원들로부터 때때로 교묘하게 조종하거나 기만적이라는 비
 유튜브, 정치인·공직자·언론인을 대상으로 AI 딥페이크 탐지 기능 확대
화요일, 유튜브는 딥페이크 탐지 기술을 일부 정부 관계자, 정치 후보자 및 언론인 대상으로 확대한다고 발표했다. 이 도구는 AI로 생성된 유사 영상을 식별하며, 시범 운영 참여자들은 유튜브 정책을 위반한다고 판단되는 무단 콘텐츠의 삭제를 요청할 수 있다.이 탐지 시스템은 초기 테스트 단계를 거친 후, 작년 유튜브 파트너 프로그램에 가입된 약 400만 명의
유튜브, 정치인·공직자·언론인을 대상으로 AI 딥페이크 탐지 기능 확대
화요일, 유튜브는 딥페이크 탐지 기술을 일부 정부 관계자, 정치 후보자 및 언론인 대상으로 확대한다고 발표했다. 이 도구는 AI로 생성된 유사 영상을 식별하며, 시범 운영 참여자들은 유튜브 정책을 위반한다고 판단되는 무단 콘텐츠의 삭제를 요청할 수 있다.이 탐지 시스템은 초기 테스트 단계를 거친 후, 작년 유튜브 파트너 프로그램에 가입된 약 400만 명의
AlphaFold 3 sounds like a game-changer! Predicting molecular interactions could speed up drug discovery big time. Curious how it stacks up against traditional lab methods. 🧬
AlphaFold 3 sounds like a game-changer! Predicting molecular interactions with such precision could really speed up drug discovery. I'm curious how it stacks up against traditional lab methods in terms of cost and time. Anyone know? 🤔
AlphaFold 3 sounds like a game-changer! Predicting molecular interactions could speed up drug discovery big time. Excited to see how it shapes medical breakthroughs! 🚀
AlphaFold 3 sounds like a game-changer! Predicting molecular interactions could speed up drug discovery big time. Curious how it stacks against human researchers—will it outsmart us or just make our coffee breaks longer? 😄
AlphaFold 3 sounds like a game-changer! Predicting molecular interactions with such precision could unlock new frontiers in medicine. But I wonder, will this tech stay accessible to all researchers, or get locked behind paywalls? 🤔


















 집
집























